One World una pelea
─ Cooperación internacional para construir una comunidad global de destino común que responda a la pandemia de Covid-19
La novela coronavirus que se extiende en todo el mundo ha resultado en una crisis pandemia global de 19 Covid-19 en curso. La novela coronavirus no tiene fronteras, no se salvará de esta batalla contra Covid-19. En respuesta a esta pandemia mundial de Covid-19, Liming BioProducts Corp está haciendo contribuciones para apoyar el bienestar de nuestras comunidades globales.
Nuestro mundo se enfrenta actualmente al impacto sin precedentes de la nueva pandemia de la enfermedad del coronavirus 2019 (Covid-19). Hasta la fecha, no hay fármaco eficiente disponible para el tratamiento de esta enfermedad. Sin embargo, se han desarrollado muchas pruebas de diagnóstico para la detección de COVID-19. Estas pruebas se basan en métodos moleculares o serológicos para detectar los nuevos biomarcadores de ácido nucleico o anticuerpos específicos de coronavirus. Como Covid-19 ha alcanzado un estado de pandemia, el diagnóstico temprano de la nueva infección por coronavirus es fundamental para evaluar la propagación del virus y contenerlo, pero aún no existe una prueba perfecta para el uso universal. Tenemos que saber qué pruebas podrían usarse potencialmente para el examen, el diagnóstico y el monitoreo de la infección Covid-19, y cuáles son sus limitaciones. Es muy importante cómo hacer un mejor uso de estas herramientas científicas y ayudar a identificar y controlar la aparición de esta enfermedad de rápida propagación y seria.
El propósito de la detección del nuevo coronavirus es determinar si un individuo que tiene infección Covid-19 o un portador asintótico que puede propagar el virus en silencio, para proporcionar información esencial para guiar la toma de decisiones para el tratamiento clínico. Estudios anteriores han demostrado que el 70% de las decisiones clínicas dependen de los resultados de las pruebas. Cuando se utilizan diferentes métodos de detección, los requisitos de los kits de reactivo de detección también son diferentes.
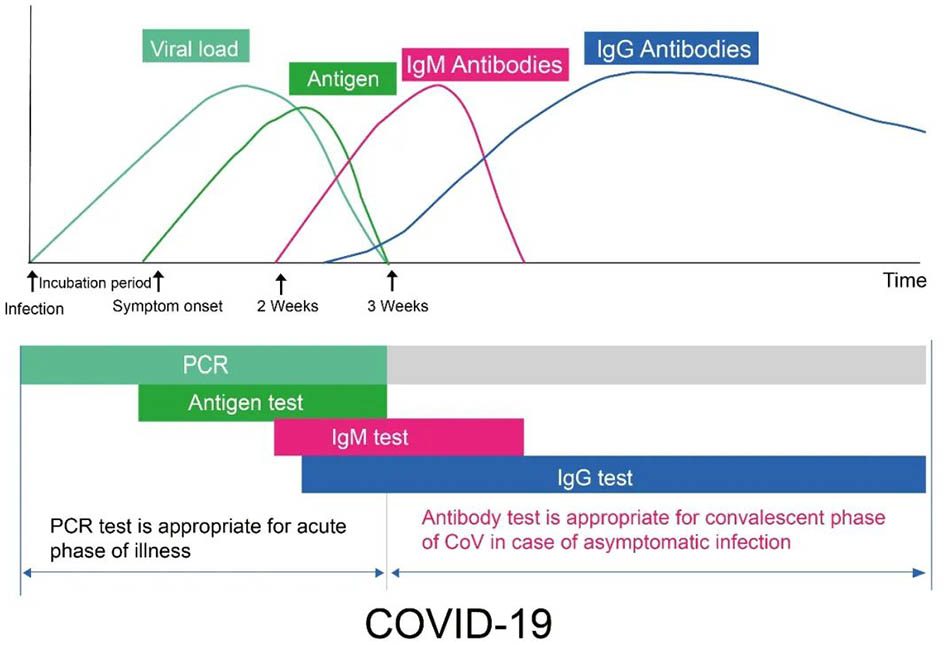
Figura 1
Figura 1:Diagrama que muestra las etapas clave de los niveles generales de biomarcadores durante el curso de tiempo típico de la infección Covid-19. El eje x indica el número de días de infección, y el eje y indica la carga viral, la concentración de antígenos y la concentración de anticuerpos en diferentes períodos. El anticuerpo se refiere a los anticuerpos IgM e IgG. Tanto la RT-PCR como la detección de antígeno se utilizan para detectar la presencia o ausencia de coronavirus novedoso, que es evidencia directa de la detección temprana del paciente. Dentro de una semana de infección viral, se prefiere la detección de PCR o la detección de antígeno. Después de la nueva infección por coronavirus durante aproximadamente 7 días, el anticuerpo IgM contra el nuevo coronavirus ha aumentado gradualmente en la sangre del paciente, pero la duración de la existencia es corta y su concentración disminuye rápidamente. En contraste, el anticuerpo IgG contra el virus aparece más tarde, generalmente aproximadamente 14 días después de la infección del virus. La concentración de IgG aumenta gradualmente, y persiste un largo período en la sangre. Por lo tanto, si el IgM se detecta en la sangre del paciente, significa que el virus se ha infectado recientemente, que es un marcador de infección temprana. Cuando el anticuerpo IgG se detecta en la sangre del paciente, significa que la infección viral ha sido durante algún tiempo. También se llama infección tardía o infección previa. A menudo se observa en pacientes que están en la fase de recuperación.
Los biomarcadores de la novela coronavirus
El novedoso coronavirus es un virus de ARN, que se compone de proteínas y ácidos nucleicos. El virus invade el cuerpo del huésped (humano), ingresa a las células a través del sitio de unión correspondiente receptor ACE2 y se replica en las células huésped, lo que hace que el sistema inmune humano responda a invasores extraños y produzca anticuerpos específicos. Por lo tanto, los ácidos y antígenos nucleicos viales, y los anticuerpos específicos contra el coronavirus novedoso pueden usarse teóricamente como biomarcadores específicos para la detección del nuevo coronavirus. Para la detección de ácido nucleico, la tecnología RT-PCR es la más utilizada, mientras que los métodos serológicos se usan comúnmente para la detección de los nuevos anticuerpos específicos de coronavirus. Actualmente, hay una variedad de métodos de prueba disponibles que podemos elegir para probar la infección de Covid-19 [1].
Principios básicos de los principales métodos de prueba para novedosos coronavir
Hasta ahora, muchas pruebas de diagnóstico para CoVID_19 están disponibles, con más kits de prueba que reciben aprobación bajo una autorización de uso de emergencia todos los días. Aunque los desarrollos de nuevas pruebas que salen con tantos nombres y formatos diferentes, todas las pruebas actuales de Covid_19 se basan básicamente en dos tecnologías principales: la detección de ácido nucleico para el ARN viral y los inmunoensayos serológicos que detectan anticuerpos específicos virales (IGM e IgG).
01. Detección de ácido nucleico
La reacción en cadena de la polimerasa de transcripción inversa (RT-PCR), la amplificación isotérmica mediada por bucle (LAMP) y la secuenciación de próxima generación (NGS) son los métodos comunes de ácido nucleico para la detección de ARN de coronavirus novedoso. RT-PCR es el primer tipo de prueba para COVID-19, recomendada por la Organización Mundial de la Salud (OMS) y el Centro de Control y Prevención de Enfermedades de los Estados Unidos (CDC).
02. Detección de anticuerpos serológicos
El anticuerpo es una proteína protectora producida en el cuerpo humano en respuesta a la infección por virus. El IGM es un tipo temprano de anticuerpo, mientras que IgG es un anticuerpo de tipo posterior. La muestra de suero o plasma generalmente se examina para detectar la presencia de tipos específicos de IgM e IgG del anticuerpo para la evaluación de fases agudas y convalecientes de la infección Covid-19. Estos métodos de detección basados en anticuerpos incluyen ensayo de inmunocromatografía de oro coloidal, inmunocromatografía de microesferas de látex o fluorescentes, ensayo de inmunosorbente ligado a enzimas (ELISA) y ensayo de quimioluminiscencia.
03. Detección de antígeno viral
El antígeno es una estructura en el virus reconocida por el cuerpo humano que desencadena el sistema de defensa inmune para producir anticuerpos para eliminar el virus de la sangre y los tejidos. Un antígeno viral presente en el virus puede dirigirse y detectarse utilizando inmunoensayo. Al igual que el ARN viral, los antígenos virales también están presentes en el tracto respiratorio de individuos infectados y pueden usarse para diagnosticar la fase aguda de la infección Covid-19. Por lo tanto, a menudo se recomienda recolectar muestras respiratorias superiores, como saliva, hisopos nasofaríngea y orofaríngeo, esputo de tos profundo, líquido de lavado broncoalveolar (BALF) para la prueba de antígeno inicial.
Selección de métodos de prueba para novedosos coronavir
La selección de un método de prueba implica muchos factores, que incluyen un entorno clínico, control de calidad de prueba, tiempo de respuesta, costos de prueba, métodos de recolección de muestreo, requisitos técnicos de personal de laboratorio, requisitos de instalaciones y equipos. La detección de ácidos nucleicos o antígenos virales es proporcionar evidencia directa de la presencia de los virus y confirmar el diagnóstico de una nueva infección por coronavirus. Aunque existen muchos métodos para la detección de antígeno, su sensibilidad de detección del nuevo coronavirus es teóricamente menor que la de la amplificación RT-PCR. La prueba de anticuerpos es la detección de anticuerpos antivirus producidos en el cuerpo humano, que está rezagado en el tiempo y, a menudo, no puede usarse para la detección temprana durante la fase aguda de la infección por virus. El entorno clínico para aplicaciones de detección puede variar, y los sitios de recolección de muestras también pueden ser diferentes. Para la detección de ácidos y antígenos nucleicos virales, la muestra debe recolectarse en el tracto respiratorio donde el virus está presente, como los hisopos nasofaríngea, los hisopos orofaríngea, el esputo o el líquido broncoalveolar (balf). Para la detección basada en anticuerpos, la muestra de sangre necesita ser recolectada y examinada para detectar la presencia de anticuerpo antivirus específico (IgM/IgG). Sin embargo, los resultados de la prueba de anticuerpos y ácido nucleico pueden complementarse entre sí. Por ejemplo, cuando el resultado de la prueba es el ácido nucleico negativo, negativo de IgM pero positivo para IgG, estos resultados indican que el paciente actualmente no lleva el virus, pero se ha recuperado de la nueva infección por coronavirus. [2]
Ventajas y desventajas de nuevas pruebas de coronavirus
En el protocolo de diagnóstico y tratamiento para la nueva neumonía por coronavirus (versión de prueba 7) (publicado por la Comisión Nacional de Salud y la Administración Estatal de Medicina China tradicional el 3 de marzo de 2020), las pruebas de ácido nucleico se usan como método estándar de oro para el diagnóstico de la novela La infección por coronavirus, mientras que las pruebas de anticuerpos también se consideran uno de los métodos de confirmación para el diagnóstico.

Hallazgos patógenos y serológicos
(1) Hallazgos patogénicos: el nuevo ácido nucleico del coronavirus se puede detectar en hisopos nasofaríngales, esputo, secreciones del tracto respiratorio inferior, sangre, heces y otras muestras utilizando métodos RT-PCRAND/o NGS. Es más preciso si las muestras se obtienen del tracto respiratorio inferior (extracción de esputo o tracto de aire). Las muestras deben enviarse para su prueba lo antes posible después de la recolección.
(2) Hallazgos serológicos: el IgM específico del virus NCP se vuelve detectable alrededor de 3-5 días después del inicio; IgG alcanza una titulación de al menos un aumento de 4 veces durante la convalecencia en comparación con la fase aguda.
Sin embargo, la selección de métodos de prueba depende de ubicaciones geográficas, regulaciones médicas y entornos clínicos. En los EE. UU., El NIH emitió la enfermedad de Coronavirus Enf. 2019 (COVID-19) Pautas de tratamiento (Sitio actualizado: 21 de abril de 2020) y la Política emitida por la FDA para las pruebas de diagnóstico para la enfermedad de Coronavirus-2019 durante la emergencia de salud pública (emitida el 16 de marzo de 2020. ), en el que las pruebas serológicas de los anticuerpos IgM/IgG seleccionados solo como prueba de detección.
Método de detección de ácido nucleico
RT_PCR es una prueba de ácido nucleico altamente sensible diseñada para detectar si el nuevo ARN de coronavirus está presente en la muestra respiratoria u otra muestra. Un resultado positivo de la prueba de PCR significa la presencia de ARN de coronavirus novedoso en la muestra para confirmar la infección COVID-19. Un resultado negativo de la prueba de PCR no significa la ausencia de la infección del virus porque podría verse afectado por la mala calidad de la muestra o el punto de tiempo de la enfermedad en la fase recuperada, etc. Aunque RT-PCR es una prueba altamente sensible, tiene varios inconvenientes. Las pruebas de RT-PCR pueden ser intensivas en mano de obra y lentas, dependiendo crucialmente de la alta calidad de la muestra. Esto puede ser un desafío porque la cantidad de ARN viral no solo varía enormemente entre diferentes pacientes, sino que también puede variar dentro del mismo paciente dependiendo de los puntos de tiempo cuando se recolecte la muestra, así como las fases de infección o el inicio de los síntomas clínicos. La detección del nuevo coronavirus requiere muestras de alta calidad que contienen una cantidad suficiente de ARN viral intacto.
La prueba RT-PCR puede dar un resultado negativo incorrecto (falso negativo) para algunos pacientes que tienen infección COVID-19. Como sabemos, los principales sitios de infección de la novela coronavirus se encuentran en el pulmón y el tracto respiratorio inferior, como los alvéolos y los bronquios. Por lo tanto, la muestra de esputo de una tos profunda o el fluido de lavado broncoalveolar (BALF) considerado que tiene la mayor sensibilidad para la detección viral. Sin embargo, en la práctica clínica, las muestras a menudo se recogen del tracto respiratorio superior utilizando hisopos nasofaríngea o orofaríngeo. La recolección de estos especímenes no solo es incómodo para los pacientes, sino que también requiere personal especialmente capacitado. Para hacer que el muestreo sea menos invasivo o más fácil, en algunos casos, a los pacientes se les puede dar un hisopo oral y permitirles tomar una muestra de la mucosa bucal o la lengua que se follan. Sin suficiente ARN viral, RT-QPCR puede devolver un resultado de la prueba falsa negativa. En la provincia de Hubei, China, la sensibilidad de RT-PCR en la detección inicial se informó solo alrededor del 30%-50%, con un promedio del 40%. La alta tasa de falsos negativos probablemente fue causada por un muestreo insuficiente.
Además, la prueba RT-PCR requiere personal altamente capacitado para realizar pasos complejos de extracción de ARN y procedimiento de amplificación de PCR. También requiere un mayor nivel de protección de bioseguridad, instalaciones de laboratorio especial e instrumento de PCR en tiempo real. En China, la prueba RT-PCR para la detección de COVID-19 debe realizarse en los laboratorios de nivel 2 de bioseguridad (BSL-2), con protección del personal que utiliza la práctica del nivel 3 de bioseguridad (BSL-3). Según estos requisitos, desde principios de enero hasta principios de febrero de 2020, la capacidad del laboratorio de CDC de China Wuhan solo pudo detectar unos pocos cientos de casos por día. Normalmente, esto no sería un problema al probar otras enfermedades infecciosas. Sin embargo, cuando se trata de una pandemia global como Covid-19 con potencialmente millones de personas para ser probadas, RT-PCR se convierte en un problema crítico debido a sus requisitos para las instalaciones de laboratorio especiales o equipos técnicos. Estas desventajas pueden limitar la RT-PCR a ser utilizada como una herramienta eficiente para la detección, y también pueden conducir a retrasos en los informes de los resultados de las pruebas.
Método de detección de anticuerpos serológicos
Con el progreso del curso de la enfermedad, especialmente en las etapas media y tardía, la tasa de detección de anticuerpos es muy alta. Un estudio en el Hospital Wuhan Central South mostró que la tasa de detección de anticuerpos podría alcanzar más del 90% en la tercera semana de infección Covid-19. Además, el anticuerpo es el producto de la respuesta inmune humana contra el coronavirus novedoso. La prueba de anticuerpos ofrece varias ventajas sobre RT-PCR. En primer lugar, el anticuerpo serológico prueba simple y rápido. Las pruebas de flujo lateral de anticuerpos se pueden usar para el punto de atención para entregar un resultado en 15 minutos. En segundo lugar, el objetivo detectado por la prueba serológica es el anticuerpo, que se sabe que es mucho más estable que el ARN viral. Durante la recolección, transporte, almacenamiento y pruebas, las muestras para las pruebas de anticuerpos son generalmente más estables que las muestras para RT-PCR. En tercer lugar, debido a que el anticuerpo se distribuye uniformemente en la circulación sanguínea, hay menos variación de muestreo en comparación con la prueba de ácido nucleico. El volumen de muestra requerido para la prueba de anticuerpos es relativamente pequeño. Por ejemplo, 10 microlitros de sangre de huella dedo son suficientes para su uso en la prueba de flujo lateral del anticuerpo.
En general, la prueba de anticuerpos se elige como una herramienta de suplemento para la detección de ácido nucleico para mejorar la tasa de detección del nuevo coronavirus durante los cursos de enfermedad. Cuando la prueba de anticuerpos se usa junto con una prueba de ácido nucleico, puede aumentar la precisión del ensayo para el diagnóstico de CoVID19 al reducir los posibles resultados falsos positivos y falsos negativos. La Guía de operación actual no recomienda usar dos tipos de prueba por separado como formato de detección independiente, pero debe usarse como un formato combinado. [2]
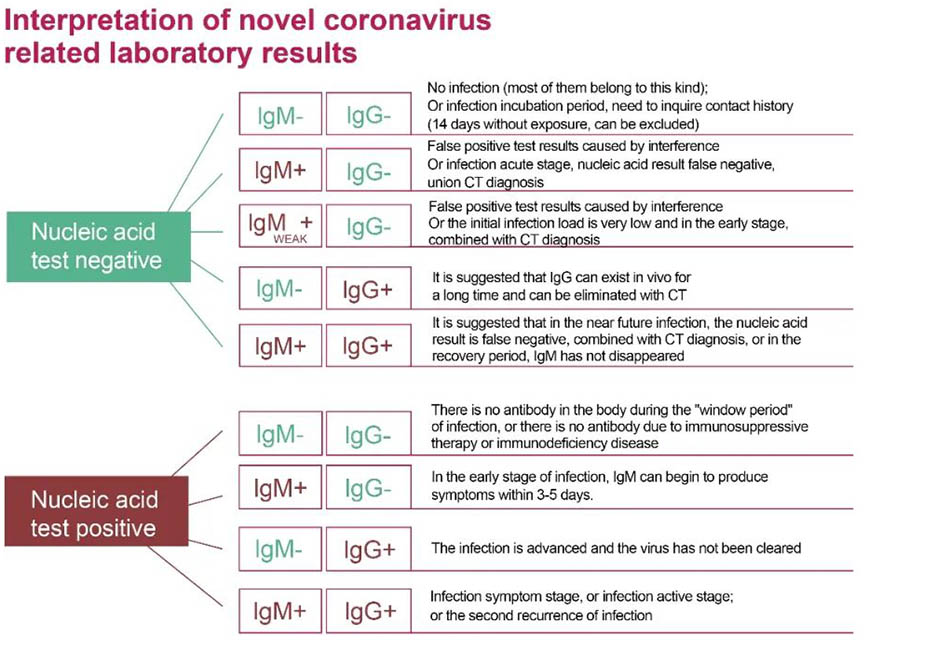
Figura 2:La interpretación correcta del ácido nucleico y los resultados de la prueba de anticuerpos para la detección de una nueva infección por coronavirus

Figura 3:Liming Bio-Products Co., Ltd.-Nuevo kit de prueba rápida de anticuerpo IgG IgM/IgG (StrongStep®Prueba rápida de anticuerpos SARS-CoV-2 IgG/IgG, inmunocromatografía de látex)

Figura 4:Liming Bio-Products Co., Ltd.-Strongstep®El nuevo kit de PCR en tiempo real de Coronavirus (SARS-COV-2) (detección para tres genes, método de sonda fluorescente).
Nota:Este kit de PCR altamente sensible y listo para usar está disponible en formato liofilizado (proceso de liofilización) para el almacenamiento a largo plazo. El kit se puede transportar y almacenar a temperatura ambiente y es estable durante un año. Cada tubo de premix contiene todos los reactivos necesarios para la amplificación de PCR, incluida la transcriptasa inversa, la polimerasa Taq, los cebadores, las sondas y los sustratos DNTPS. Los usuarios simplemente pueden reconstituir la mezcla agregando agua de rentancia de PCR junto con la plantilla y luego cargar en un instrumento de PCR para ejecutar la amplificación.
En respuesta al nuevo brote de coronavirus, Liming Bio-Products Co., Ltd. ha trabajado rápidamente para desarrollar dos kits de diagnóstico para permitir que los laboratorios de salud clínica y pública diagnostican rápidamente la infección de Covid-19. Estos kits son muy adecuados para su uso para la detección a gran escala en países y regiones donde el nuevo brote de coronavirus se está propagando rápidamente y para proporcionar diagnóstico y confirmación para la infección de CoVID-19. Estos kits son para su uso solo bajo la autorización de uso de emergencia pre-notificada (PEUA). Las pruebas se limitan a los laboratorios certificados bajo las regulaciones de las autoridades nacionales o locales.
Método de detección de antígeno
1. La detección de antígeno viral se clasifica en la misma categoría de detección directa que la detección de ácido nucleico. Estos métodos de detección directa buscan evidencia de patógenos virales en la muestra y pueden usarse para el diagnóstico de confirmación. Sin embargo, el desarrollo de kits de detección de antígeno requiere una alta calidad de anticuerpos monoclonales con una fuerte afinidad y alta sensibilidad capaz de reconocer y capturar virus patógenos. Por lo general, lleva más de seis meses seleccionar y optimizar un anticuerpo monoclonal adecuado para su uso en la preparación del kit de detección de antígeno.
2. Actualmente, los reactivos para la detección directa de la novela coronavirus todavía están en etapa de investigación y desarrollo. Por lo tanto, ningún kit de detección de antígeno ha sido clínicamente validado y disponible comercialmente. Aunque previamente se informó que una empresa de diagnóstico en Shenzhen ha desarrollado un kit de detección de antígeno y se probó clínicamente en España, la confiabilidad y precisión del ensayo no se pudo validar debido a la presencia de problemas de calidad de reactivos. Hasta la fecha, NMPA (ex FDA de China) no ha aprobado ningún kit de detección de antígeno para uso clínico. En conclusión, se han desarrollado una variedad de métodos de detección. Cada método tiene sus ventajas y limitaciones. Los resultados de diferentes métodos se pueden utilizar para la verificación y el complemento.
3. Producir un kit de prueba Covid-19 de calidad depende en gran medida de la optimización durante la investigación y el desarrollo. Liming Bio-Product Co., Ltd. Se requieren kits de prueba para cumplir con los estrictos estándares de fabricación y control de calidad para garantizar que proporcionen los niveles más altos de rendimiento y consistencia. Los científicos de Liming Bio-Product Co., Ltd. tienen más de veinte años de experiencia en el diseño, las pruebas y la optimización de kits de diagnóstico in vitro para garantizar el más alto nivel de rendimiento en la cuantificación analítica.
Durante la pandemia de Covid-19, el gobierno chino enfrentó una oleada de la gran demanda de materiales de prevención epidémica en los puntos críticos internacionales. El 5 de abril, en la conferencia de prensa del mecanismo de prevención y control del Consejo de Estado "Fortalecer la gestión de calidad de los materiales médicos y regular el orden del mercado", Jiang Fan, inspector de primer nivel del Departamento de Comercio Exterior del Ministerio del Ministerio del comercio, dijo: "A continuación, centraremos nuestros esfuerzos en dos aspectos, primero, para acelerar el apoyo de más suministros médicos que necesitan la comunidad internacional y también para mejorar el control de calidad, la regulación y la gestión de los productos. Haremos la contribución de China para responder conjuntamente a la epidemia global y construir una comunidad con un futuro compartido para la humanidad.



Figura 5:El nuevo reactivo Coronavirus de Liming Bio-Products Co., Ltd. ha obtenido el certificado de registro de la UE CE
El certificado honorario


Houshenshan
Figura 6. Liming Bio-Products Co., Ltd. apoyó al Hospital de Montaña Wuhan Vulcan (Houshenshan) para luchar contra la epidemia Covid-19 y recibió el certificado honorario de la Cruz Roja de Wuhan. El Hospital Wuhan Vulcan Mountain es el hospital más famoso de China que se especializa en el tratamiento de Covid severo: 19 pacientes.
A medida que el brote de coronavirus novedoso continúa extendiéndose en todo el mundo, Nanjing liming Bio-Products Co., Ltd. está dando un paso adelante para apoyar y ayudar a las comunidades de todo el mundo con nuestras tecnologías innovadoras para combatir esta amenaza global sin precedentes. Las pruebas rápidas de la infección de Covid-19 son una parte crítica para abordar esta amenaza. Continuamos contribuyendo de manera significativa al proporcionar plataformas de diagnóstico de alta calidad en manos de los trabajadores de la salud de primera línea para que las personas puedan recibir los resultados críticos de las pruebas que necesitan. Los esfuerzos de Liming Bio-Products Co., Ltd. en la batalla contra la pandemia Covid-19 son contribuir con nuestras tecnologías, experiencias y experiencia a las comunidades internacionales para la construcción de una comunidad global de destino.
Long Press ~ Scan y síguenos
Correo electrónico: sales@limingbio.com
Sitio web: https://limingbio.com
Tiempo de publicación: mayo-01-2020







