Dispositivo del sistema StrongStep para prueba rápida de antígeno SARS-CoV-2
Uso previsto
Dispositivo del sistema StrongStep® para la prueba rápida de antígeno SARS-CoV-2 emplea tecnología de inmunocromatografía para detectar el antígeno nucleocapsido SARS-CoV-2 en la saliva humana. Esta prueba es solo de uso único y está destinada a SEI, probando. Se recomienda utilizar esta prueba dentro de los 7 días posteriores al inicio de los síntomas, está respaldado por la evaluación del rendimiento clínico.
INTRODUCCIÓN
Los novedosos coronavirus pertenecen al género 0. Covid-19 es una enfermedad infecciosa respiratoria aguda. Las personas son generalmente susceptibles. Actualmente, los pacientes infectados por el nuevo coronavirus son la principal fuente de infección basada en la investigación epidemiológica actual, el período de incubación es de 1 a 14 días, principalmente de 3 a 7 días. Las manifestaciones principales incluyen fiebre, fatiga y tos seca. La congestión nasal, la secreción nasal, el dolor de garganta, la mialgia y la diarrea se encuentran en algunos casos.
PRINCIPIO
El dispositivo del sistema StrongStep® para la prueba de antígeno SARS-CoV-2 emplea una prueba inmunocromatográfica, este kit recolecta muestras de saliva del palo de adsorción de saliva en la parte delantera de la tarjeta de prueba, y las muestras de saliva avanzan bajo la acción capilar. Si la muestra contiene un antígeno de proteína SARS-CoV-2 N, se identifica y está unido por anticuerpos marcados en la superficie del látex para formar un complejo inmune. Cuando el complejo inmune formado migra a la línea de detección de membrana de fibra de ácido nítrico, para identificar los anticuerpos empaquetados y formar una línea de detección de fucsia (T-Lins), que muestra un antígeno SARS-CoV-2 positivo; Si la línea T no muestra color, es un resultado negativo. Otra línea en la membrana de fibra de ácido nítrico está lleno de anticuerpos por estreptavidina como una línea de control de calidad (línea C), para indicar un proceso de prueba efectivo.
PRECAUCIONES
• Este kit es solo para uso de diagnóstico in vitro.
• Este kit puede ser administrado por personal médico o no médico siguiendo las instrucciones de funcionamiento.
• Lea las instrucciones cuidadosamente antes de realizar la prueba.
• Este producto no contiene ningún material fuente humano.
• No use el contenido del kit después de la fecha de vencimiento.
• Manejar todas las muestras como potencialmente infecciosas.
• No pipette reactivo por vía oral y no haya fumar ni comer mientras realiza ensayos.
• Use guantes durante todo el procedimiento.
Almacenamiento y estabilidad
Las bolsas selladas en el kit de prueba se pueden almacenar entre 2-30 ° C durante la duración de la vida útil como se indica en la bolsa.
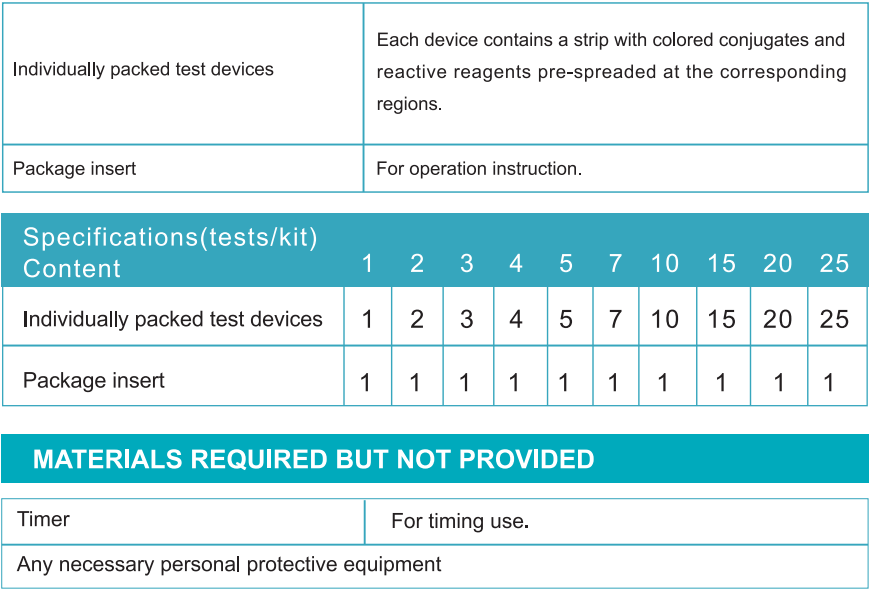
Colección y almacenamiento de muestras
El mejor espécimen de saliva debe recolectarse por la mañana después de despertarse. No coma ni beba nada durante 30 minutos antes de recolectar su muestra de saliva. Hágalo antes de tomar un café, desayunar o cepillarse los dientes, o esperar hasta que no haya consumido nada en los 30 minutos anteriores.
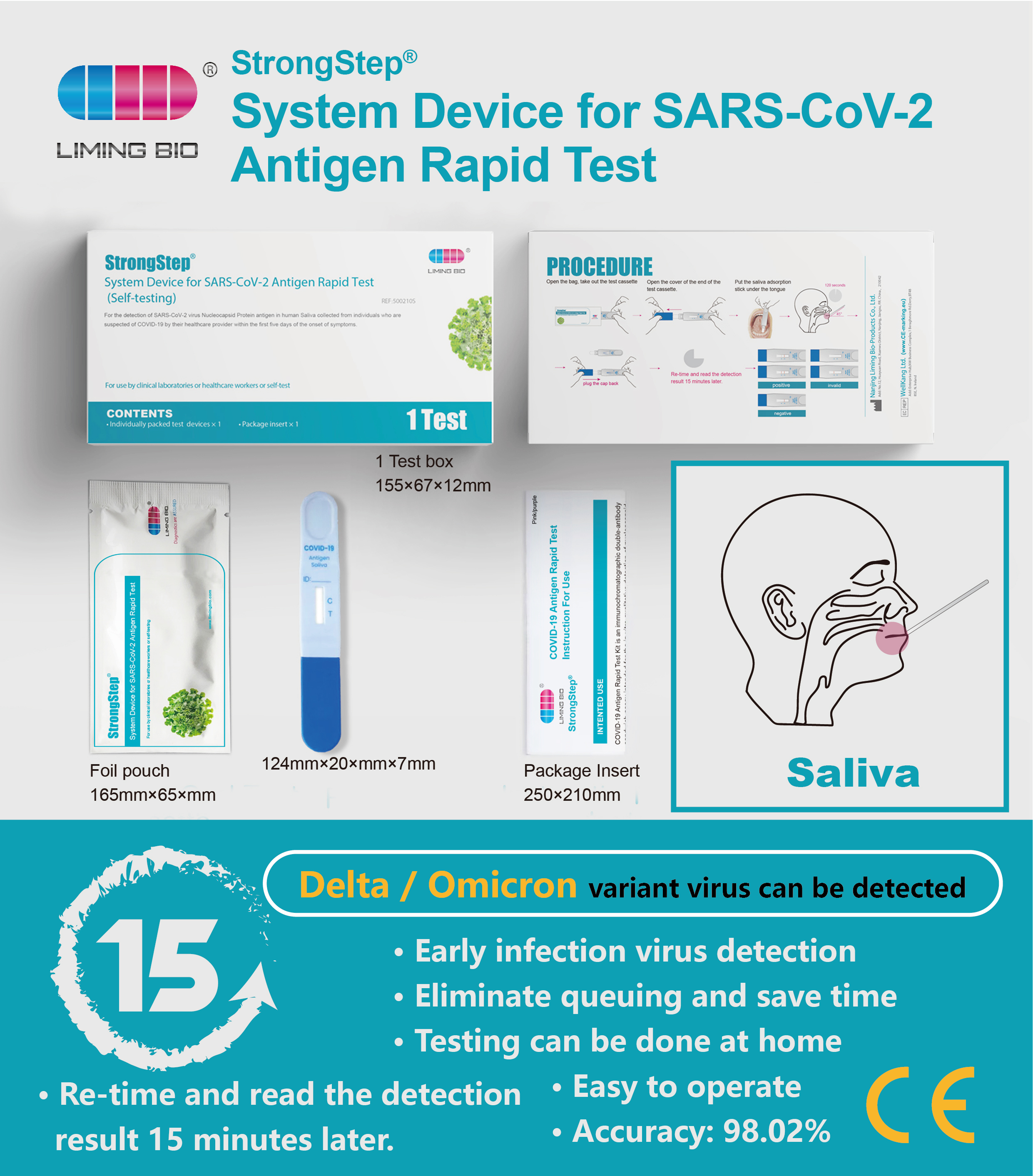
PROCEDIMIENTO
Traiga las pruebas a temperatura ambiente (15-30 ° C) antes de su uso.
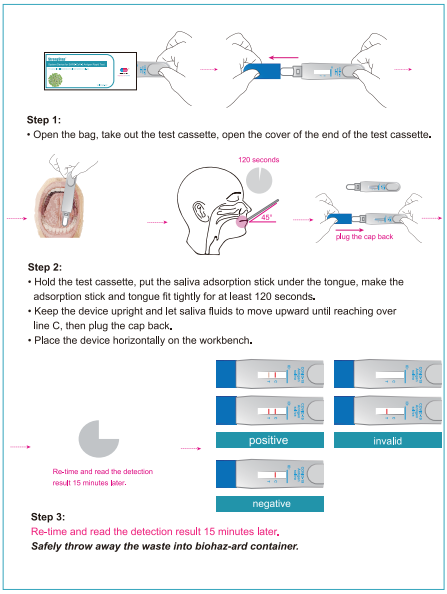
Paso 1:
Abra la bolsa, saque el dispositivo de prueba, abra la cubierta del final del dispositivo de prueba.
Paso 2:
• Sostenga el cassette para no, coloque el palo de adsorción de saliva debajo de la lengua, haga que el palo de adsorción y la lengua se ajusten firmemente durante al menos 120 segundos.
• Mantenga el dispositivo en posición vertical y deje que los fluidos de la saliva se muevan hacia arriba hasta que se extienda sobre la línea C, luego conecte la tapa hacia atrás.
• Coloque el dispositivo horizontalmente en el banco de trabajo.
Paso 3:
Realice el tiempo y lea la detección resuh 15 minutos después.
Deseche con seguridad los desechos en un contenedor biohaz-ardor.
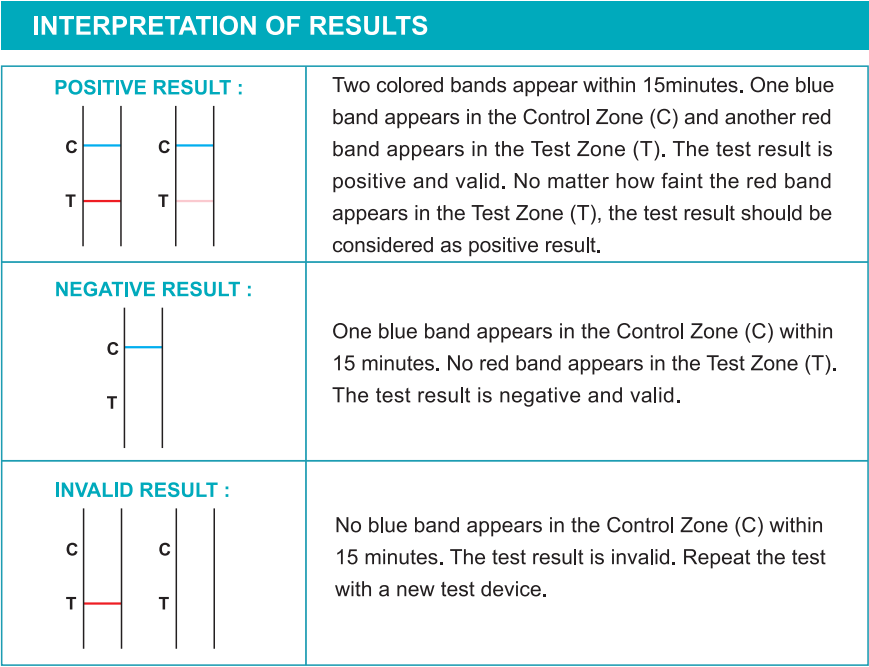
CONTROL DE CALIDAD
Los controles de procedimiento internos se incluyen en la prueba. Una banda azul que aparece en la región de control (c) se considera un control de procedimiento interno. Confirma suficiente volumen de muestras y una técnica de procedimiento correcta.
Limitaciones de la prueba
1. El kit está destinado a usar para la detección cualitativa de antígenos SARS-CoV-2 de la saliva.
2. Esta prueba detecta SARS-CoV-2 viable (vivo) y no viable. El rendimiento de la prueba depende de la cantidad de virus (antígeno) en la muestra y puede o no correlacionarse con los resultados del cultivo viral realizados en la misma muestra.
3. Un resultado negativo de la prueba puede ocurrir si el nivel de antígeno en una muestra está por debajo del límite de detección de la prueba o si la muestra fue recolectada o transportada de manera incorrecta.
4. El fracaso para seguir el procedimiento de prueba puede afectar negativamente el rendimiento de la prueba y/o invalidar el resultado de la prueba.
5. El kit es solo para la detección de presuntos. Los resultados negativos no descartan la infección SARS-CoV-2 y la persona que no es infecciosa. Si hay síntomas presentes, busque pruebas inmediatas.
6. Los resultados de las pruebas deben correlacionarse con el historial clínico, los datos epidemiológicos y otros datos disponibles para el clínico que evalúa al paciente.
7. Los resultados positivos de la prueba no descartan coinfecciones con otros patógenos y no necesariamente no pueden determinar si una persona es infecciosa.
8. Los resultados de las pruebas negativas no tienen la intención de gobernar en otras infecciones virales o bacterianas no SARS.
9. Los resultados negativos de los pacientes con síntoma, deben tratarse como presuntivos y confirmarse con un ensayo molecular autorizado local de la FDA, si es necesario, para el tratamiento clínico, incluido el control de infecciones.
10. Las recomendaciones de estabilidad de la muestra se basan en datos de estabilidad de las pruebas y el rendimiento de la influenza pueden ser diferentes con SARS-CoV-2. Los usuarios deben probar muestras lo más rápido posible después de la recopilación de muestras.
11. La sensibilidad para el ensayo RT-PCR en el diagnóstico de CoVID-19 es solo del 50% -80% debido a la mala calidad de la muestra o el punto de tiempo de la enfermedad en la fase de recuperación, etc. Sars-Cov-2 Antígeno La sensibilidad del dispositivo de prueba rápido es teóricamente más bajo debido a su metodología.
12. Los valores predictivos positivos y negativos dependen en gran medida de las tasas de prevalencia.
Los resultados de las pruebas positivas tienen más probabilidades de representar resultados falsos positivos durante los períodos de pequeña / no actividad SARS-CoV-2 cuando la prevalencia de la enfermedad es baja. Los resultados de las pruebas negativas es más probable cuando la prevalencia de la enfermedad causada por SARS-CoV-2 es alta.
13. Los anticuerpos monoclonales pueden no detectar o detectar con menos sensibilidad, virus de influenza SARS-CoV-2 que han sufrido cambios de aminoácidos menores en la región del epítopo objetivo.
14. El rendimiento de esta prueba no se ha evaluado para su uso en pacientes sin signos y síntomas de infección respiratoria y rendimiento puede diferir en individuos asintomáticos.
15. La cantidad de antígeno en una muestra puede disminuir a medida que aumenta la duración de la enfermedad.
Las muestras recolectadas después del día 7 de enfermedad tienen más probabilidades de ser negativas en comparación con un ensayo RT-PCR.
Se sabe que la sensibilidad de la prueba después de los siete días del inicio de los síntomas disminuye en comparación con un ensayo RT-PCR.
16. No se recomienda utilizar la muestra de medios de transporte de virus (VTM) en esta prueba, si los clientes insisten en usar este tipo de muestra, los clientes deben validarse.
17. Las pruebas frecuentes son necesarias para aumentar la sensibilidad del diagnóstico de CoVID-19.
18. Sin dejar la sensibilidad en comparación con el tipo salvaje con respecto a las siguientes variantes -B.1.1.7; B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Los resultados positivos indican que los antígenos virales se detectaron en la muestra tomada, por favor, la autónomo e informar a su médico de familia de inmediato y/o a su departamento de salud local de acuerdo con los requisitos estatales.
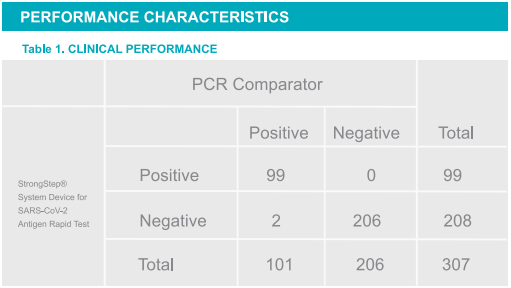
Porcentaje positivo de acuerdo: (PPA) = 98.02%(93.03%~ 99.76%)*
Porcentaje negativo de acuerdo: (NPA) = 100%(98.23%~ 100%)*
Tasa de coincidencia total = 98.76%
*Intervalo de confianza del 95%
Rendimiento analítico
a) Límite de detección (LOD):
El límite de detección (LOD) de la prueba se determinó utilizando diluciones limitantes de SARS-CoV-2 inactivados. Es una preparación de Coronavirus-2 (SARS-CoV-2) relacionado con SARS, aislando en los CDC de China, que ha sido inactivado por la β-propiolactona. El material se suministró congelado a una concentración de TCID50de 5.00 x105/ml.
Para determinar el SARS-CoV-2 para reflejar el ensayo cuando se usa saliva directa. En este estudio, aproximadamente 50 μl de la dilución del virus se dispararon con la muestra negativa de saliva.
El LOD se determinó en tres pasos:
1. Detección de LOD
Se realizaron 10 veces diluciones del virus inactivado en saliva negativa y se procesaron para cada estudio como se describió anteriormente. Estas diluciones se probaron por triplicado. La concentración que demuestra 3 de 3 positivos se eligió para el hallazgo de rango LOD.
2. Hallazgo de rango LOD
Se hicieron cinco (5) diluciones de duplicación del TCID50de 5.00 x102/concentración de ml en saliva negativa procesada para el estudio como se describió anteriormente. Estas diluciones se probaron por triplicado. La concentración que demuestra 3 de 3 positivos se eligió para la confirmación de LOD.
3. Confirmación de LOD
La concentración tcid50de 2.50 x102/ml de dilución se probó para un total de veinte (20) resultados. Al menos diecinueve (19) de veinte (20) resultados fueron positivos.
Conclusión:
Según esta prueba, la concentración se confirmó como:
LOD: TCID502.50 x102/ml
b) Reactividad cruzada:
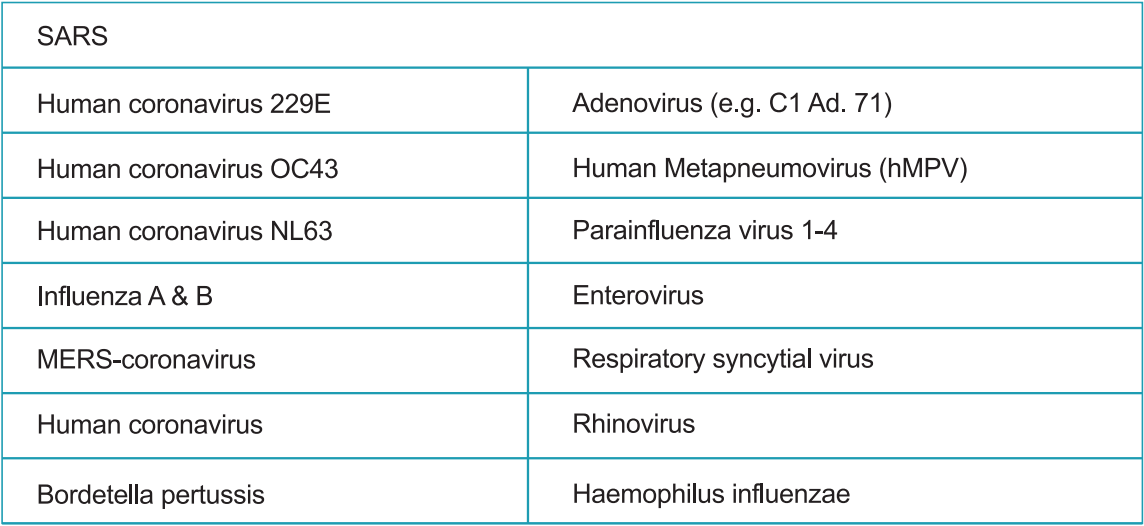
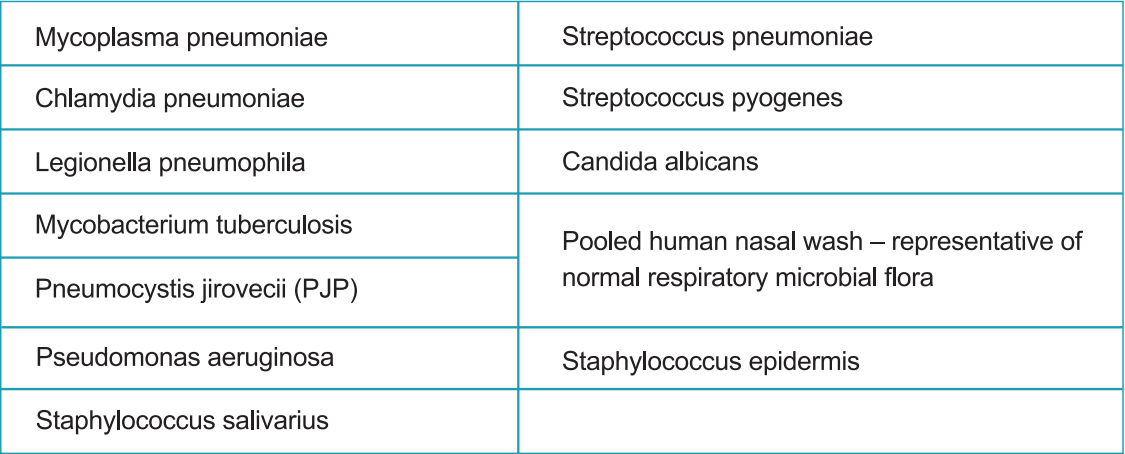
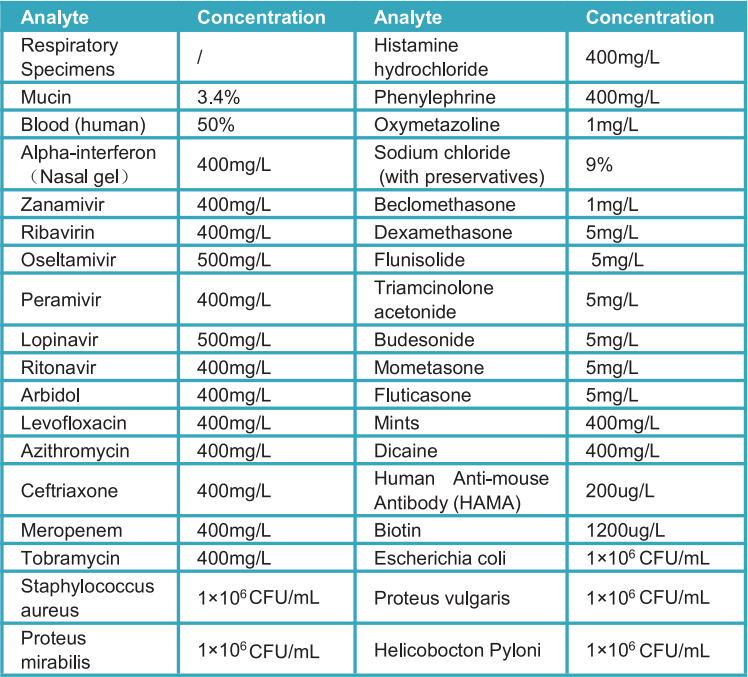
La reactividad cruzada de la prueba rápida del antígeno SARSSTEP® del dispositivo SARS-CoV-2 se evaluó probando varios microorganismos (10⁶ CFU/ml), virus (10⁵ PFU/ml) y matrices negativas que pueden reaccionar con el StrongStep® Dispositivo del sistema SARS-CoV-2 Prueba rápida de antígeno.
Cada organismo y virus se probaron por triplicado. Según los datos generados por este estudio, el dispositivo del sistema StrongStep® para la prueba rápida de antígeno SARS-CoV-2 no reacciona cruzado con los organismos o virus probados.
c) Interferir sustancia:
Las sustancias interferentes potenciales de la prueba rápida de antígeno SARGSTEP® SARS-COV-2 se evaluó probando varias sustancias con concentración por debajo que pueden interferir potencialmente con la prueba rápida de antígeno SARGSTEP® SARS-COV-2. Cada sustancia se probó por triplicado. Según los datos generados por este estudio, la prueba rápida de antígeno StrongStep® SARS-CoV-2 no interfiere con las sustancias probadas.
d) efecto de gancho
La mayor concentración de stock SARS-CoV-2 inactivado por calor disponible (TCID50de 5.00 x 105/ml) fue probado. No hubo un efecto de gancho detectado.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)