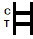Prueba rápida de graduación
Uso previsto
El strongstep®La prueba PROM es una prueba inmunocromatográfica cualitativa visualmente interpretada para la detección de IGFBP-1 del líquido amniótico en secreciones vaginales durante el embarazo. La prueba está destinada al uso profesional para ayudar a diagnosticar la ruptura de las membranas fetales (ROM) en mujeres embarazadas.
INTRODUCCIÓN
La concentración de IGFBP-1 (proteína de unión al factor de crecimiento similar a la insulina-1) en el líquido amniótico es de 100 a 1000 veces mayor que en suero materno. IGFBP-1 generalmente no está presente en la vagina, pero después de la ruptura de las membranas fetales, el fluido amniótico con una alta concentración de IGFBP-1 se mezcla con secreciones vaginales. En la prueba de graduación StrongStep®, se toma una muestra de secreción vaginal con un hisopo de poliéster estéril y la muestra se extrae en la solución de extracción de muestras. La presencia de IGFBP-1 en la solución se detecta utilizando un dispositivo de prueba rápido.
PRINCIPIO
El strongstep®La prueba de graduación utiliza la tecnología de flujo capilar de color inmunocromatográfico de color. El procedimiento de prueba requiere la solubilización de IGFBP-1 de un hisopo vaginal mezclando el hisopo en el tampón de muestra. Luego, el búfer de muestra mixto se agrega bien a la muestra de casete de prueba y la mezcla migra a lo largo de la superficie de la membrana. Si IGFBP-1 está presente en la muestra, formará un complejo con el anticuerpo primario anti-IGFBP-1 conjugado con partículas de color. El complejo estará unido por un segundo anticuerpo anti-IGFBP-1 recubierto con la membrana de nitrocelulosa. La aparición de una línea de prueba visible junto con la línea de control indicará un resultado positivo.
Componentes del kit
| 20 Individualmente PackDispositivos de prueba ED | Cada dispositivo contiene una tira con conjugados de color y reactivos reactivos previamente recubiertos en las regiones correspondientes. |
| 2ExtracciónVial búfer | 0,1 m de solución salina tamponada con fosfato (PBS) y azida de sodio al 0,02%. |
| 1 hisopo de control positivo (solo a pedido) | Contienen IGFBP-1 y azida de sodio. Para control externo. |
| 1 hisopo de control negativo (solo a pedido) | No contener IGFBP-1. Para control externo. |
| 20 Tubos de extracción | Para el uso de preparación de muestras. |
| 1 Puesto de trabajo | Coloque para sostener viales y tubos de búfer. |
| 1 Inserto de paquete | Para la instrucción de operación. |
Materiales requeridos pero no proporcionados
| Minutero | Para uso de tiempo. |
PRECAUCIONES
■ Solo para uso de diagnóstico in vitro profesional.
■ No use después de la fecha de vencimiento indicada en el paquete. No use la prueba si su bolsa de lámina está dañada. No reutilice las pruebas.
■ Este kit contiene productos de origen animal. El conocimiento certificado del origen y/o el estado sanitario de los animales no garantiza totalmente la ausencia de agentes patógenos transmisibles. Por lo tanto, se recomienda que estos productos se traten como potencialmente infecciosos y se manejen observando las precauciones de seguridad habituales (no ingieran ni inhale).
■ Evite la contaminación cruzada de muestras mediante el uso de un nuevo contenedor de recolección de muestras para cada muestra obtenida.
■ Lea el procedimiento completo cuidadosamente antes de realizar cualquier prueba.
■ No coma, beba ni fume en el área donde se manejan las muestras y los kits. Manejar todas las muestras como si contengan agentes infecciosos. Observe las precauciones establecidas contra los riesgos microbiológicos a lo largo del procedimiento y siga los procedimientos estándar para la eliminación adecuada de las muestras. Use ropa protectora como capas de laboratorio, guantes desechables y protección para los ojos cuando se analizan las muestras.
■ No intercambie ni mezcle reactivos de diferentes lotes. No mezcle las tapas de las botellas de solución.
■ La humedad y la temperatura pueden afectar negativamente los resultados.
■ Cuando se complete el procedimiento de ensayo, deseche los hisopos cuidadosamente después de autoclárselo a 121 ° C durante al menos 20 minutos. Alternativamente, pueden tratarse con hipocloruro de sodio al 0,5% (o blanqueador de la casa) durante una hora antes de la eliminación. Los materiales de prueba utilizados deben descartarse de acuerdo con las regulaciones locales, estatales y/o federales.
■ No use cepillos de citología con pacientes embarazadas.
Almacenamiento y estabilidad
■ El kit debe almacenarse a 2-30 ° C hasta la fecha de vencimiento impresa en la bolsa sellada.
■ La prueba debe permanecer en la bolsa sellada hasta su uso.
■ No se congele.
■ Se deben tomar cuidado para proteger los componentes en este kit de la contaminación. No use si hay evidencia de contaminación microbiana o precipitación. La contaminación biológica de los equipos, contenedores o reactivos de dispensación puede conducir a falsos resultados.
Colección y almacenamiento de muestras
Use solo hisopos estériles con punta de dacron o rayón con ejes de plástico. Se recomienda utilizar el hisopo suministrado por el fabricante de kits (los hisopos no están contenidos en este kit, para la información de pedido, comuníquese con el fabricante o el distribuidor local, el número de catálogo es de 207000). Los hisopos de otros proveedores no han sido validados. No se recomiendan hisopos con puntas de algodón o ejes de madera.
■ Se obtiene una muestra utilizando un hisopo de poliéster estéril. La muestra debe recolectarse antes de realizar un examen digital y/o ultrasonido transvaginal. Tenga cuidado de no tocar nada con el hisopo antes de tomar la muestra. Inserte cuidadosamente la punta del hisopo en la vagina hacia el fornix posterior hasta que se cumpla la resistencia. Alternativamente, la muestra se puede tomar del fórnix posterior durante un examen de especulo estéril. El hisopo debe dejarse en la vagina durante 10-15 segundos para permitir que absorba la secreción vaginal. ¡Saca el hisopo con cuidado!.
■ Coloque el hisopo en el tubo de extracción, si la prueba se puede ejecutar de inmediato. Si no es posible las pruebas inmediatas, las muestras del paciente deben colocarse en un tubo de transporte seco para el almacenamiento o el transporte. Los hisopos se pueden almacenar durante 24 horas a temperatura ambiente (15-30 ° C) o 1 semana a 4 ° C o no más de 6 meses a -20 ° C. Se debe permitir que todas las muestras alcancen una temperatura ambiente de 15-30 ° C antes de la prueba.
PROCEDIMIENTO
Traiga pruebas, muestras, tampón y/o controles a temperatura ambiente (15-30 ° C) antes de su uso.
■ Coloque un tubo de extracción limpio en el área designada de la estación de trabajo. Agregue 1 ml de tampón de extracción al tubo de extracción.
■ Coloque el espécimen de hisopo en el tubo. Mezcle vigorosamente la solución girando el hisopo con fuerza contra el costado del tubo durante menos diez veces (mientras está sumergido). Los mejores resultados se obtienen cuando la muestra se mezcla enérgicamente en la solución.
■ Exprima la mayor cantidad de líquido posible del hisopo pellizcando el lado del tubo de extracción flexible a medida que se retira el hisopo. Al menos 1/2 de la solución de tampón de muestra debe permanecer en el tubo para que se produzca una migración capilar adecuada. Coloque la tapa en el tubo extraído.
Deseche el hisopo en un contenedor de desechos biohazartos adecuados.
■ Las muestras extraídas pueden retener a temperatura ambiente durante 60 minutos sin afectar el resultado de la prueba.
■ Retire la prueba de su bolsa sellada y colóquela en una superficie limpia y nivelada. Etiquete el dispositivo con identificación de paciente o control. Para obtener un mejor resultado, el ensayo debe realizarse dentro de una hora.
■ Agregue 3 gotas (aproximadamente 100 µl) de la muestra extraída del tubo de extracción al pozo de muestra en el casete de prueba.
Evite atrapar burbujas de aire en el pozo (s) de muestra y no deje caer ninguna solución en la ventana de observación.
A medida que la prueba comienza a funcionar, verá que el color se mueve a través de la membrana.
■ Espere a que aparezcan las bandas de colores. El resultado debe leerse a los 5 minutos. No interprete el resultado después de 5 minutos.
Deseche los tubos de ensayo usados y los casetes de prueba en un contenedor de desechos biohazartos adecuados.
Nterpretación de resultados
| POSITIVORESULTADO:
| Aparecen dos bandas de colores en la membrana. Una banda aparece en la región de control (c) y otra banda aparece en la región de prueba (t). |
| NEGATIVORESULTADO:
| Solo aparece una banda de color en la región de control (C). No aparece ninguna banda de color aparente en la región de prueba (t). |
| INVÁLIDORESULTADO:
| La banda de control no aparece. Los resultados de cualquier prueba que no haya producido una banda de control en el tiempo de lectura especificado debe descartarse. Revise el procedimiento y repita con una nueva prueba. Si el problema persiste, suspenda con el kit de inmediato y comuníquese con su distribuidor local. |
NOTA:
1. La intensidad del color en la región de prueba (t) puede variar según la concentración de sustancias dirigidas presentes en la muestra. Pero el nivel de sustancias no se puede determinar mediante esta prueba cualitativa.
2. Volumen de muestra insuficiente, procedimiento de operación incorrecto o realización de pruebas caducadas son las razones más probables para la falla de la banda de control.
CONTROL DE CALIDAD
■ Los controles de procedimiento internos se incluyen en la prueba. Una banda de color que aparece en la región de control (c) se considera un control de procedimiento positivo interno. Confirma suficiente volumen de muestras y una técnica de procedimiento correcta.
■ Los controles de procedimiento externos pueden proporcionar (solo a pedido) en los kits para garantizar que las pruebas funcionen correctamente. Además, los controles pueden usarse para demostrar el rendimiento adecuado por parte del operador de prueba. Para realizar una prueba de control positiva o negativa, complete los pasos en la sección del procedimiento de prueba tratando el hisopo de control de la misma manera que un hisopo de muestras.
Limitaciones de la prueba
1. No se debe hacer una interpretación cuantitativa en función de los resultados de la prueba.
2. No use la prueba si su bolsa de aluminio de aluminio o los sellos de la bolsa no están intactos.
3.Un Positive Strongstep®El resultado de la prueba de graduación, aunque detectar la presencia de líquido amniótico en la muestra, no localiza el sitio de la ruptura.
4. Como con todas las pruebas de diagnóstico, los resultados deben interpretarse a la luz de otros hallazgos clínicos.
5. Si se ha producido una ruptura de las membranas fetales, pero la fuga de líquido amniótico ha cesado más de 12 horas antes de que se tome la muestra, IGFBP-1 puede haber sido degradada por proteasas en la vagina y la prueba puede dar un resultado negativo.
Características de rendimiento
Tabla: Strongstep®Prueba de graduación vs. otra prueba de graduación de marca
|
Sensibilidad relativa: |
| Otra marca |
| ||
| + | - | Total | |||
| Fuerte®PASEO Prueba | + | 63 | 3 | 66 | |
| - | 2 | 138 | 140 | ||
|
| 65 | 141 | 206 | ||
Sensibilidad analítica
La cantidad detectable más baja de IGFBP-1 en la muestra extraída es de 12.5 μg/L.
Sustancias interferentes
Se debe tener cuidado para no contaminar el aplicador o las secreciones cervicovaginales con lubricantes, jabones, desinfectantes o cremas. Los lubricantes o cremas pueden interferir físicamente con la absorción de la muestra en el aplicador. Los jabones o desinfectantes pueden interferir con la reacción de anticuerpo-antígeno.
Las sustancias interferentes potenciales se probaron en concentraciones que podrían encontrarse razonablemente en las secreciones cervicovaginales. Las siguientes sustancias no interfirieron en el ensayo cuando se probaron en los niveles indicados.
| Sustancia | Concentración | Sustancia | Concentración |
| Ampicilina | 1.47 mg/ml | Prostaglandina F2 | 0.033 mg/ml |
| Eritromicina | 0.272 mg/ml | Prostaglandina E2 | 0.033 mg/ml |
| Orina materna 3er trimestre | 5% (vol) | Monistatr (Miconazol) | 0.5 mg/ml |
| Oxitocina | 10 iu/ml | Carmín índigo | 0.232 mg/ml |
| Terbutalino | 3.59 mg/ml | Gentamicina | 0.849 mg/ml |
| Dexametasona | 2.50 mg/ml | Gel betadiner | 10 mg/ml |
| Mgso4•7H2O | 1.49 mg/ml | Betadiner limpiador | 10 mg/ml |
| Ritodrino | 0.33 mg/ml | Gelatina de K-años | 62.5 mg/ml |
| Dermicidolr 2000 | 25.73 mg/ml |
Referencias de literatura
Erdemoglu y Mungan T. Importancia de la detección del factor de crecimiento similar a la proteína de unión al factor de crecimiento 1 en las secreciones cervicovaginales: comparación con la prueba de nitrazina y la evaluación del volumen de líquidos amnióticos. Acta Obstet Gynecol Scand (2004) 83: 622-626.
Kubota T y Takeuchi H. Evaluación de la proteína de unión al factor de crecimiento similar a la insulina como una herramienta de diagnóstico para la ruptura de las membranas. J Obstet Gynecol Res (1998) 24: 411-417.
Rutanen EM et al. Evaluación de una prueba de tira rápida para la proteína de unión al factor de crecimiento similar a la insulina-1 en el diagnóstico de membranas fetales rotas. Clin Chim Acta (1996) 253: 91-101.
Rutanen EM, Pekonen F, Karkkainen T. Medición de la proteína de unión al factor de crecimiento similar a la insulina-1 en secreciones cervicales/vaginales: comparación con el inmunoensayo de membrana de verificación ROM en el diagnóstico de membranas fetales rupidas. Clin Chim Acta (1993) 214: 73-81.
Glosario de símbolos
|
| Número de catálogo |  | Limitación de temperatura |
 | Consulte las instrucciones para su uso |
| Código por lotes |
 | Dispositivo médico de diagnóstico in vitro |  | Usar |
 | Fabricante |  | Contiene suficiente para |
 | No reutilice |  | Representante autorizado en la comunidad europea |
 | CE marcado de acuerdo con la Directiva de dispositivos médicos IVD 98/79/CE | ||